|
|
back
MENU
|
|
Private
|

Polymeres
4.10 ISOLANTS NATURELS ET INORGANIQUES DE SYNTHESE
4.10.1 Introduction
Les matériaux diélectriques utilisés aujourd'hui sont extrêmement nombreux et variés. Différents critères peuvent être envisagés pour les classer, tel que leur état : solide, liquide ou gazeux, leur origine : naturelle ou artificielle, etc.. Quel que soit le critère retenu, la place très importante des diélectriques organiques de synthèse nécessite de les traiter à part. Ils font l'objet des sections 4.11 à 4.14. La présente section est donc consacrée globalement à tous les autres diélectriques.
Devant l'ampleur de la matière, il ne peut être question ici que de traiter succinctement de quelques diélectriques parmi les plus importants.
4.10.2 Céramiques
Les céramiques sont des substances dures et souvent cassantes, présentant généralement une juxtaposition de phase cristalline et amorphes. Elles sont fabriquées à partir de silicate d'alumine, de silicate de magnésium, de quartz, d'alumine, de dioxyde de titane, etc.. La pièce à exécuter est tout d'abord réalisée par moulage, les matériaux devant la constituer se présentant sous forme de poudre. (Ce moulage est, provisoirement, rendu suffisamment résistant mécaniquement par la présence de liants adéquats). Elle passe ensuite dans un four, pour y subir un traitement thermique appelé frittage au cours duquel les liants seront éliminés et les grains agglomérés. Le frittage présente la caractéristique de se dérouler à une température inférieure à la température de fusion des constituants. Au cours de ce traitement, les grains s'annexent mutuellement et progressivement par deux processus de surface, intervenant aux points de contact dès que la température est suffisamment élevée. Premièrement, la diffusion aux points de contact initiaux provoque un réarrangement des atomes aboutissant à la formation de petites aires de contact, de dimensions croissantes. Deuxièmement, la sublimation sur les surfaces voisines des aires de contact fournit des atomes supplémentaires coopérant à l'augmentation de ces dernières. En effet, le courant de particules émises par sublimation est plus élevé sur une surface convexe que sur une surface concave sur laquelle les atomes sont liés davantage (fig. 4.46).
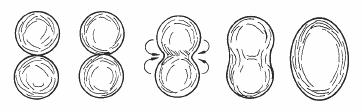
Fig. 4.46 Représentation schématique des étapes successives de la réunion de deux grains par frittage
Le frittage se produit entre 1200C et 1500C selon les composants, et s'accompagne d'un retrait de 10 à 20% . Il est donc difficile de respecter des tolérances dimensionnelles serrées. Les seules possibilités d'usinage sont le meulage et le polissage à la poudre de diamant ou de carbure de silicium. Les trous peuvent être forés par ultrasons. Souvent poreuses, les céramiques peuvent être recouvertes d'une couche vitreuse assurant l'étanchéité et la protection contre la pollution. Une couche de métallisation permet la fixation par soudage de pièces métalliques.
Les céramiques résistent aux courants superficiels et aux arcs. Elles conservent leurs bonnes propriétés électriques jusque vers 1 000C. Elles ne vieillissent pas et sont très résistantes aux agents chimiques, acide phosphorique concentré et acide fluorhydrique exceptés. Elles sont coûteuses.
On classe les céramiques en fonction de leur composition.
Avec 40 à 50% de silicate d'alumine, 30 à 40% de quartz, 20 à 30% de feldspath (silicate double d'aluminium et de potassium, ou d'un autre métal alcalin) on obtient une porcelaine formée de cristaux de quartz et de silicate d'aluminium enrobés dans une masse amorphe. Cette céramique est utilisée pour les isolateurs de grandes dimensions.
Avec 70 à 90%de silicate de magnésium, 5 à 10% de silicate d'alumine, 5 à 10% de feldspath on obtient une céramique formée de silicate de magnésium cristallisé enrobé dans une masse amorphe. Elle est utilisée en haute fréquence et comme support pour les résistances à film ou bobinées.
En adjoignant aux silicates d'alumine et de magnésium, des composés de titane tels que le dioxyde de titane, le titanate de magnésium ou de baryum, on obtient des céramiques à permittivité très élevée, utilisées pour la fabrication de condensateurs de petites dimensions.
Les céramiques à haute teneur en alumine (50 à 80%) sont employées comme substrats pour la confection de circuits intégrés hybrides à couches épaisses, car les dépôts métalliques y adhèrent convenablement.
4.10.3 Composés organiques naturels
Par leur nombre, ils forment une catégorie importante, à laquelle appartiennent le papier, les huiles minérales, la paraffine, diverses cires comme l'ozokérite, la colophane, le coton, etc. Tous ces produits ont tendance à être remplacés par des composés organiques de synthèse. L'évolution est plus lente en ce qui concerne le papier, dont la porosité reste une propriété originale intéressante permettant une imprégnation par divers agents, tels que des huiles. Son caractère hygroscopique est par contre un inconvénient.
4.10.4 Gaz électronégatifs
On appelle gaz électronégatifs, ceux dont les molécules contiennent des atomes d'halogènes. La structure électronique particulière des halogènes ( 1.2.13) confère à ces gaz une certaine affinité pour les électrons, qui inhibe fortement le développement des décharges.
Parmi ces gaz, l'hexafluorure de soufre SF6, disponible sur une base industrielle et d'un coût abordable, est le plus largement utilisé. Sa rigidité à 60 Hz, sous la pression atmosphérique, est comparée à celle de l'air sec et d'autres composés fluorés moins courants sur les figures 4.47 et 4.48.
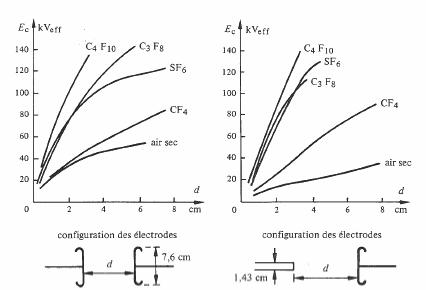
Fig. 4.47 Ec en champ homogène, d'après [63] Fig. 4.48 Ec en champ inhomogène, d'après [63]
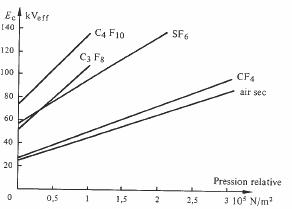
Fig. 4.49 D'après [63].
L'augmentation de Ec en fonction de la pression, à 60 Hz et pour la configuration d'électrodes de la figure 4.47 avec d = 1,27 cm est représentée à la figure 4.49. En champ inhomogène, Ec peut diminuer quand la pression augmente, pour certains gaz électronégatifs et dans certaines gammes de pression.
Ces quelques caractéristiques suffisent à démontrer les qualités remarquables du SF6. Ce gaz est utilisé, pur ou dilué dans l'azote, dans divers dispositifs à haute tension et en particulier dans les disjoncteurs, dont il permet de diminuer fortement les dimensions.
4.11 ISOLANTS ORGANIQUES DE SYNTHÈSE. INTRODUCTION AUX POLYMÈRES
4.11.1 Chimie organique, rappels et définitions
La chimie organique a pour objet l'étude des composés formés de carbone et d'hydrogène, plus éventuellement d'autres éléments tels que l'azote, l'oxygène, le phosphore, le soufre, certains métaux et halogènes. Les substances organiques sont extrêmement variées et nombreuses. On en connaît plus d'un million à l'heure actuelle. Leur étude et leur nomenclature sont simplifiées par le fait que l'on peut reconnaître dans les molécules organiques, certains assemblages d'atomes se retrouvant dans un grand nombre de molécules différentes. Ces assemblages, véritables briques de la chimie organique, sont appelés groupes ou groupements. Le plus simple est le groupe hydroxyle, constitué d'un atome hydrogène et d'un atome oxygène et noté - OH pour indiquer qu'il offre un lien de valence.
4.11.2 Groupements dans les hydrocarbures
Les hydrocarbures sont des composés formés exclusivement de carbone et d'hydrogène. Les groupements qu'on peut déceler dans ces substances sont les groupements hydrocarbonés. Leur nom dérive le plus souvent de celui de l'hydrocarbure correspondant (tab. 4.50 et 4.51). Il existe plusieurs classes d'hydrocarbures dont deux seulement sont mentionnées ici, en raison de leur relation avec les isolants présentés plus loin. Ce sont :
• les hydrocarbures aliphatiques, dont l'ossature est une chaîne ouverte d'atomes de carbone. On appelle alcanes les hydrocarbures aliphatiques ne présentant pas de double ou triple liaison entre atomes de carbone.
• les hydrocarbures aromatiques, caractérisés par le fait qu'ils contiennent au moins un cycle hexagonal à trois doubles liaisons.
Les groupements dérivant d'alcanes constituent la famille des alkyles, souvent désignés par le symbole général R.
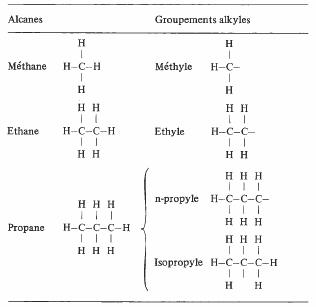
Tableau 4.50 Les trois alcanes les plus simples et les groupements
alkyles correspondants. Deux groupements dérivent du propane.
On les distingue par un préfixe.
Les groupements dérivant d'hydrocarbures aromatiques sont les aryles, souvent désignés par le symbole général Ar (tab. 4.51).
4.11.3 Polymères, définitions
Certaines molécules simples ont la propriété, sous des conditions physio-chimiques appropriées, de s'unir les unes aux autres pour former des molécules plus grandes, constituant une répétition dans l'espace de la molécule initiale. On appelle polymérisation ce type de réaction et polymère la substance qui en résulte. Par le terme de monomère, on désigne la molécule et donc la substance de départ.
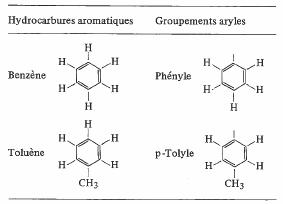
Tableau 4.51 Deux hydrocarbures aromatiques très simples et les groupements aryles correspondants.
Divers procédés de polymérisation sont utilisés.
• Dans la polymérisation en masse, on place simplement le monomère dans une enceinte, en ajoutant éventuellement des catalysateurs. Généralement, la réaction ne peut avoir lieu que sous des pressions et températures élevées. L'appareillage utilisé est donc complexe. Le polymère présente une pureté élevée.
• Dans la polymérisation en solution le monomère, et les catalyseurs s'il y a lieu, sont dissous dans un solvant. Ce procédé permet d'opérer à des températures plus basses et d'extraire plus efficacement la chaleur de réaction. Comparé à la polymérisation en masse, il nécessite une opération supplémentaire : la séparation du polymère et du solvant. Par ailleurs, les impuretés du solvant sont susceptibles de polluer le polymère.
• La polymérisation en émulsion est caractérisée par le fait que les substances en présence pour la réaction forment deux phases non miscibles. Le polymère se forme soit dans l'une des phases, soit à la surface de séparation des phases.
On distingue deux types de réactions de polymérisation.
• On appelle polymérisation par addition, (ou polyaddition) l'assemblage des monomères sans formation d'un produit de réaction. La formation du polyéthylène ( 4.12.1) par ouverture de la double liaison C = C dans l'éthylène en est un exemple typique.
• Dans les cas où un produit de réaction est formé, le caoutchouc silicone ( 4.13.2) en est un exemple, on parle de polymérisation par condensation, ou polycondensation.
4.11.4 Structure moléculaire des polymères, définitions
Un polymère formé d'un seul type de monomère est appelé homopolymère. S'il comprend deux monomères différents ou davantage, c'est un copolymère.
Un homopolymère peut présenter trois structures différentes (tab. 4.52).
Les structures d'un copolymère sont plus nombreuses et plus complexes que celles d'un homopolymère, car elles dépendent encore de la disposition régulière ou aléatoire des différents monomères le long des chaînes.
La structure moléculaire des polymères influence de façon décisive leurs propriétés mécaniques.
Tableau 4.52 Représentation schématique
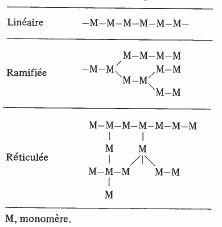
Aux structures linéaires et faiblement ramifiées, correspondent les thermoplastiques (sect. 4.12). Comme leur nom l'indique, ces substances se déforment facilement quand la température augmente, ce qui s'explique par les liaisons faibles (type Van der Waals ( 1.3.16)) reliant les chaînes voisines. On peut agir sur ces liaisons au moyen de plastifiants, qui sont des substances diminuant encore l'énergie de liaison entre chaînes.
Aux structures faiblement réticulées, c'est à dire formant un réseau à mailles larges, correspondent les élastomères, (sect. 4.13), dont le comportement mécanique est comparable à celui du caoutchouc.
Lorsque les mailles du réseau deviennent serrées, l'élasticité disparaît. Le matériau est appelé thermodurcissable (sect. 4.14), car la formation du réseau serré est accélérée par une élévation de température.
Localement, les structures linéaires peuvent s'aligner parallèlement les unes aux autres, constituant une zone dans laquelle la disposition des atomes devient régulière,
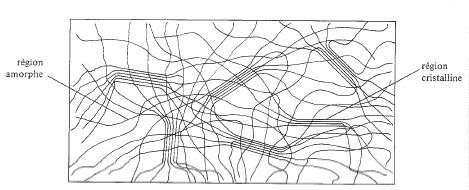
Fig. 4.53
c'est à dire cristalline (fig. 4.53). On appelle cristallinité d'un polymère, le rapport du volume de ces zones au volume total de l'échantillon.
La variation du module d'élasticité EY d'un thermoplastique en fonction de la température présente quatre stades (ou domaines) (fig. 4.54).
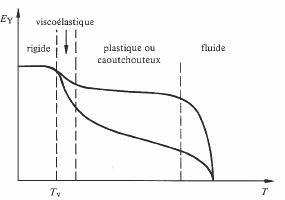
Fig. 4.54
La température en dessous de laquelle le matériau devient cassant s'appelle température de transition vitreuse Tv (6.5.2). L'existence de ces stades s'explique par le relâchement progressif de forces d'interaction entre chaînes.
4.12 THERMOPLASTIQUES
4.12.1 Polyethylene
Formée par polymérisation de l'éthylène C2H4 (fig. 4.55), la molécule de polyéthylène se présente sous la forme d'une chaîne d'atomes de carbone dont les valences libres sont occupées par des atomes hydrogène (fig. 4.15). Cette chaîne contient de 1 000 à 20 000 monomères. Le poids moléculaire de celui-ci étant de 28, celui de la molécule peut s'étendre de 30 000 à 550 000 environ. La molécule de polyéthylène peut présenter des ramifications (fig. 4.56).
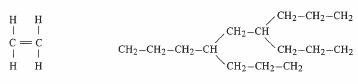
Fig. 4.55 Ethylène Fig. 4.56 Molécule de polyéthylène ramifiée
Ces ramifications provoquent une diminution de la densité du matériau et de sa cristallinité. Leur nombre est élevé quand le polyéthylène est obtenu par le procédé haute pression. Il est faible dans le polyéthylène provenant de l'un des procédés basse pression.
Comme manière première le polyéthylène s'obtient sous forme de granulés ou de poudre. Il est mis en forme par extrusion, injection, soufflage, etc. Il se travaille entre 180 et 250 C, et présente un retrait de 2 à 3% lors du refroidissement à la température ambiante. La poudre de polyéthylène est destinée aux techniques de dépôt par lit fluidisé, pulvérisation électrostatique, etc.
Comme semi-ouvré, le polyéthylène est livrable en tubes et profils divers, feuilles, rubans dont l'épaisseur descend jusqu'à 20 microns. Sous cette dernière forme, il peut remplacer le papier dont le caractère hygroscopique est gênant pour certaines applications.
Le polyéthylène peut être réticulé par un procédé physique ou chimique. Dans les deux cas il s'agit de retirer des atomes hydrogène pour provoquer des liaisons directes entre atomes de carbone appartenant à des chaînes voisines. Le procédé physique utilise l'éjection d'atomes H par irradiation aux électrons ou aux rayons X. Il s'emploie pour de faibles épaisseurs en raison des difficultés à obtenir une réticulation homogène quand les pièces deviennent massives. Le procédé chimique recourt à l'adjonction de peroxydes. Par élévation de la température après mise en forme (par extrusion p. ex.) on provoque la décomposition du peroxyde. Les radicaux libres formés à ce moment opèrent les captures d'hydrogène nécessaires.
Le polyéthylène se prête à la fabrication de tubes thermorétractables. Le processus est le suivant. Un tube est extrudé, puis dilaté par gonflage alors qu'il se trouve dans le domaine caoutchouteux. Dans cet état il est refroidi, ce qui gèle les tensions induites par sollicitation des forces de liaison entre chaînes. Lors d'une nouvelle élévation de température jusque dans le domaine caoutchouteux, ces tensions se manifesteront à nouveau, tendant à faire reprendre au tube ses dimensions primitives. Les tubes thermorétractables s'obtiennent également par irradiation. Celle-ci provoque de nouvelles liaisons entre chaînes créant également des tensions internes se manifestant dès que la température s'élève suffisamment.
Les propriétés du polyéthylène varient en fonction de sa densité, située aux alentours de 0,92 avec une cristallinité de 70% pour la qualité haute pression, et 0,96 avec une cristallinité de 93 % pour la qualité basse pression. Le module d'élasticité, la résistance à la traction, à la flexion, la dureté croissent avec la densité. Le polyéthylène basse pression est donc meilleur mécaniquement, mais la qualité haute pression est meilleure électriquement, car une cristallinité élevée est le plus souvent source d'inhomogénéités pouvant conduire à des claquages.
Le polyéthylène possède une haute rigidité diélectrique, et une bonne résistance au cheminement des décharges superficielles. La rigidité diélectrique en champ alternatif peut être augmentée par des additifs aromatiques, qui améliorent également la résistance aux décharges partielles. La permittitivité est indépendante de la fréquence jusque dans les hyperfréquences. Il en est de même de tan δ car la molécule est non polaire. La variation de εr et tan δ en fonction de la température résulte uniquement du changement de densité. Le polyéthylène est assez inerte chimiquement, mais il brûle. Le polyéthylène est très utilisé comme isolant, dans les câbles à haute fréquence (coaxiaux), et les câbles à haute tension, jusqu'à 220 kV.
4.12.2 Polychlorure de vinyle (PVC)
La molécule de polychlorure de vinyle (fig. 4.15) est obtenue par polymérisation du monomère chlorure de vinyle (fig. 4.57). La disposition aléatoire des atomes de chlores (molécule atactique), dont le diamètre est plus grand que celui des atomes d'hydrogène empêche la formation des zones cristallines : le PVC est essentiellement amorphe. Le moment dipolaire de la liaison C-CL crée des forces d'interactions dipolaires entre chaînes voisines, responsables de la rigidité mécanique du PVC.
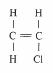 Fig. 4.57 Chlorure de vinyle.
Fig. 4.57 Chlorure de vinyle.
Plusieurs procédés de polymérisation sont utilisables. La polymérisation en masse est la plus récente, elle présente l'avantage que les restes de catalyseurs sont les seules impuretés possibles. La polymérisation en présence d'eau nécessite l'adjonction de substances favorisant la formation de suspensions ou d'émulsions, en plus des catalyseurs.
Le PVC pur est instable à la chaleur et à la lumière. Le stéarate de plomb est un stabilisant fréquemment utilisé pour améliorer sa résistance à ces agents. La température de transition vitreuse Tv du PVC est élevée, elle se situe entre 75 et 80C, ce qui le rend impropre à de nombreuses applications (câbles p. ex.) sans l'adjonction de plastifiants tels que le dioctylphtalate. Les plastifiants agissent par diminution de l'intensité des liaisons dipolaires entre chaînes voisines, et permettent de ramener Tv entre - 10C et - 5C. Des substances neutres comme la craie et le caolin peuvent être incorporées au PVC sans en altérer les propriétés d'une façon trop importante. On obtient ainsi un PVC chargé, de moindre coût par unité de volume. Dès 150C, le PVC se décompose en dégageant de l'acide chlorydrique. Placé dans une flamme il brûle, mais ne propage pas lui-même la flamme.
Disponible sous forme de poudre ou de granulés, le PVC se travaille par extrusion, injection ou calandrage, à des températures qui dépendent des additifs et du mode de mise en forme. On l'obtient également sous forme de profilés.
Il est utilisé comme gainage et isolant de câbles d'énergie (jusqu'à 10 kV environ) et de câbles de télécommunications basse fréquence. De nombreuses petites pièces isolantes sont injectées en PVC.
4.12.3 Polystyrène
Le polystyrène est un composé aromatique ; sa molécule se présente comme une molécule d'éthylène dans laquelle un atome hydrogène est remplacé par un anneau benzénique (fig. 4.58). La polymérisation en masse du styrène liquide à température ambiante, donne le polystyrène possédant les meilleures propriétés électriques. D'autres procédés de polymérisation sont également utilisables, par émulsion, précipitation, etc.
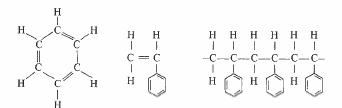
Benzène Styrène Polystyrène
Fig. 4.58
Les anneaux benzéniques se placent sur la chaîne des atomes de carbone de façon totalement désordonnée (molécule atactique) de sorte que le polystyrène n'est pas cristallin. Son poids moléculaire oscille entre 150 000 et 400 000, ce qui représente 1 500 à 4000 monomères. On devrait s'attendre à ce que le polystyrène soit fortement polaire, en raison de la grande dissymétrie introduite dans la molécule par les anneaux benzéniques. En réalité, ces derniers sont bloqués par leur taille elle-même, ce qui a deux conséquences.
Premièrement, le polystyrène est non polaire car les moments dipolaires permanents, orientés aléatoirement, sont incapables de s'aligner sous l'effet d'un champ extérieur.
Deuxièmement, le polystyrène est assez cassant et sensible aux chocs en raison de l'entrave que constitue les noyaux benzéniques au déplacement relatif de chaînes voisines. Cet inconvénient est sans importance quand le polystyrène est utilisé sous forme de feuilles minces, comme dans les condensateurs, où sa haute résistivité et ses faibles pertes diélectriques sont le mieux exploitées. On peut le rendre moins cassant en le mélangeant à un élastomère à base de butadiène, mais c'est au détriment de ses propriétés électriques.
Le polystyrène présente une résistance aux radiations ionisantes supérieures à celle de la majorité des autres thermoplastiques. Transparent, il se laisse colorer aisément. Il brûle facilement avec une odeur aromatique caractéristique. Le polystyrène est plastique dès 80C déjà et se travaille à des températures généralement inférieures à celles en usage pour d'autres thermoplastiques.
Dans la fabrication des condensateurs à diélectrique enroulé, on l'utilise sous forme de feuilles étirées à chaud, et donc thermorétractables, ce qui résout de manière élégante le problème du compactage des couches conducteur-isolant. Il est facile d'assembler par soudage des pièces en polystyrène. Cette matière se prête également très bien à l'injection de pièces d'une masse comprise entre 1 g et 10 kg, telles que les corps de bobinage, les boîtiers et supports isolants de toutes sortes. Un inconvénient du polystyrène est son prix relativement élevé.
4.12.4 Polypropylène (PP)
La molécule de polypropylène est une molécule d'éthylène dans laquelle on aurait remplacé un atome hydrogène par un groupement méthyle - CH3 (fig. 4.59). Selon le procédé de polymérisation, on obtient un polypropylène atactique ou isotactique. Seule la molécule isotactique donne un matériau intéressant pour les applications. Sa cristallinité est comprise entre 50% et 75%. Une macromolécule contient entre 6 000 et 18 000 monomères, ce qui correspond à un poids moléculaire moyen de l'ordre de 500 000.
Le polypropylène, comme le polyéthylène, est non polaire et de faible poids spécifique.
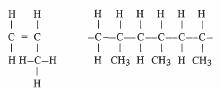
Propylène Polypropylène
Fig 4.59
Par rapport à ce dernier, il présente l'avantage d'une meilleure résistance à la traction et d'une dureté plus élevée. Malheureusement, sa température de transition vitreuse est relativement haute : - 12C. Le polypropylène sous forme de minces feuilles étirées présente la cristallinité la plus élevée et une résistance à la traction atteignant 120 à 200 N/mm2 (rupture). Dans le polypropylène massif, les propriétés mécaniques peuvent être améliorées par l'adjonction de fibres de verre ou de fibres d'amiante.
La permittivité du polypropylène est constante en fonction de la fréquence, jusqu'à 109 Hz. La seule variation de εr en fonction de la température est celle que provoque le changement de masse spécifique. La rigidité diélectrique des feuilles minces atteint 300 kV/mm. Le polypropylène brûle.
Il est couramment mis en forme par injection, à une température comprise entre 190C et 240C. Il présente un retrait de 1,5 %. Les feuilles les plus minces de 6 à 12 microns, sont obtenues par étirage de feuilles plus épaisses, à une température proche du point de fin de cristallisation.
En raison du cumul de bonnes propriétés électriques et mécaniques, le polypropylène est largement utilisé en particulier dans les domaines suivants : isolateurs d'antennes, manchons de raccordement pour câbles, boîtiers divers, ailettes de refroidissement dans les moteurs. Le polypropylène est utile en combinaison avec le papier dans les condensateurs de puissance servant à compenser la composante réactive du courant.
4.12.5 Polytetrafluoréthylène (PTFE)
Si l'on remplace les 4 atomes d'hydrogène de la molécule d'éthylène par 4 atomes de fluor, on obtient le tetrafluoréthylène, dont la polymérisation donne le polytetrafluoréthylène (fg. 4.60), largement connu sous le nom de Teflon (nom de marque de Dupont de Nemours). Les procédés de polymérisation en émulsion ou en suspension sont utilisables et livrent le polymère sous forme de poudre très fine. Le poids moléculaire est compris entre 500 000 et 5 000 000. La symétrie de la macromolécule fait du polytetrafluoréthylène un matériau non polaire d'une part, à cristallinité élevée d'autre part.
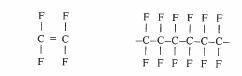
Tetrafluoréthylène Polytetrafluoréthylène
Fig. 4.60
La permittivité ne varie pas jusqu'à 1010 Hz, les pertes diélectriques, de l'ordre de 10-4 à 106 Hz n'atteignent que 5 10-4 à 109 Hz, ce qui est particulièrement faible. La résistivité est élevée et peu affectée par la présence d'humidité. Par contre, la dégradation sous l'effet de décharges (effluves, etc..) limite le champ électrique admissible.
Le domaine des températures d'utilisation en permanence est exceptionnel, puisqu'il s'étend de -200C à + 200C. Aux plus basses températures, la matière reste souple. Les propriétés mécaniques sont très moyennes. Le fluage est assez important. Le coefficient de frottement superficiel est bas.
La mise en forme du polytetrafluoréthylène diffère radicalement de celle des autres thermoplastiques, en raison d'un point de cristallisation très élevé, 327C, et de la viscosité considérable de la matière à cette température. Les procédés utilisés s'apparentent à ceux de la métallurgie des poudres. Le polytetrafluoréthylène s'usine facilement par les moyens conventionnels. On peut lui incorporer diverses charges, en particulier le dioxyde de titane TiO2, pour en abaisser le prix volumique.
Il est utilisé couramment dans les connecteurs à haute fréquence. Chargé de fibres de verre, on peut en faire des isolateurs de suspension sur lesquels la neige ne s'accumule pas. Il sert également à la confection d'espaceurs dans les câbles cryogéniques. D'une façon générale, son usage est indiqué dans les conditions thermiques extrêmes.
4.12.6 Autres thermoplastiques
Le polycarbonate (PC)(fig. 4.61) possède un poids moléculaire de 150 000 environ, il est peu cristallin.
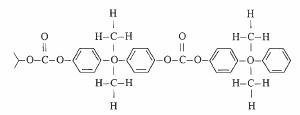
Fig. 4.61 Polycarbonate
Son importance en électrotechnique est croissante. Il résiste extrêmement bien au choc et supporte les températures relativement élevées : 120C en continu. Ses propriétés électriques sont moyennes. Les rubans de polycarbonate thermorétractable sont fréquemment utilisés pour isoler les bobinages. Des feuilles très minces, jusqu'à 2 microns, d'épaisseur constante et se prêtant bien à la métallisation par l'aluminium peuvent être obtenues, d'où l'intérêt du polycarbonate pour les condensateurs de dimensions réduites.
Les polyamides (PA) constituent un groupe important de thermoplastiques dont certains représentants comme les nylons trouvent des applications en électrotechnique, notamment quand les qualités mécaniques (dureté, résistance à l'abrasion) sont plus importantes que les qualités électriques. Ces dernières sont en particulier limitées par le caractère hygroscopique de ces matières.
Les thermoplastiques mentionnés ci-dessus sont à considérer comme des exemples parmi les matériaux les plus couramment utilisés. D'autres thermoplastiques sont décrits par exemple dans [64].
4.13 ELASTOMERES
4.13.1 Polyisoprène
Le polyisoprène (fig. 4.62) est le caoutchouc naturel. Ce polymère s'obtient également par voie de synthèse. La vulcanisation est produite par le soufre qui établit des liaisons entre chaînes voisines en faisant éclater les doubles liaisons.
La résistivité électrique du polyisoprène est élevée, mais il résiste mal aux courants superficiels. La présence de soufre le rend légèrement polaire. La température maximum admissible en permanence n'est que de 60C. Il vieillit relativement mal, et ne résiste pas à l'ozone ni à certaines huiles minérales. Les sels, les bases, l'acide sulfurique concentré et les acides organiques, à l'exception de l'acide nitrique ne l'attaquent pas.
Coûteux pour ses performances, le polyisoprène est progressivement remplacé par d'autres caoutchoucs synthétiques tels que les EPR ou les EPDM ( 4.13.4).
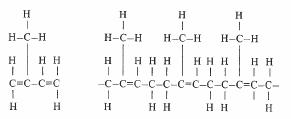
Fig. 4.62
4.13.2 Caoutchoucs silicones
Les caoutchoucs silicones sont des polymères de poids moléculaire élevé, compris entre 10 000 et 700 000. Ils se distinguent par la présence de silicium dans la chaîne principale de la molécule. Le degré de réticulation peut être facilement dosé, de sorte que ces matériaux sont susceptibles de se présenter aussi bien comme des élastomères que comme des thermodurcissables.
Les caoutchoucs silicones sont essentiellement mis en oeuvre par extrusion, injection et calandrage, la vulcanisation pouvant être provoquée (par élévation de température) dans la machine de mise en forme elle-même, ou dans une enceinte séparée.
Leur caractéristique spécifique est une excellente tenue en température, provenant de la stabilité de la liaison Si-0 constituant la chaîne principale. Ils supportent en continu des températures comprises entre -50C + 180C. Leurs qualités mécaniques sont inférieures à celles des autres élastomères, elles peuvent être améliorées par adjonction de poudre de quartz ou de dioxyde de titane. Ils sont non polaires. Ils résistent bien aux courants superficiels, leur résistivité varie peu en fonction de la température (2 ordres de grandeur environ jusqu'à 200C). Ils sont incombustibles et, même décomposés dans la chaleur d'un incendie par exemple, ils peuvent encore assurer une certaine isolation, ce qui est intéressant pour certaines installations de sécurité. La benzine, les hydrocarbures chlorés aliphatiques et les solvants aromatiques les font gonfler et perdre leurs qualités mécaniques. Ils ne supportent pas les acides et les bases concentrées, ni la vapeur d'eau au-dessus de 130C. Ils sont coûteux.
Les caoutchoucs silicones sont utilisés pour l'isolation de conducteurs et câbles. On en fait des ailettes d'isolateurs à monter sur des éléments de traction en polyépoxydes, car ils conservent de bonnes propriétés isolantes en atmosphère polluée. Ils servent à isoler divers composants haute tension et composants pour l'électronique. Ils présentent l'avantage de ne pas exercer de sollicitation mécanique sur ces composants, lors de variations de température.
4.13.3 Polyuréthanes (PU)
Les polyuréthanes possèdent des propriétés diélectriques très moyennes, insuffisantes en haute tension et haute fréquence. Leurs propriétés mécaniques sont bonnes, en particulier la résistance à l'usure, au vieillissement et aux huiles.
Le niveau de réticulation peut être varié dans de larges proportions, avec les conséquences que cela comporte concernant la dureté du produit. Certains polyuréthanes durs, se décomposant au-dessus de 320 C sont utilisés pour isoler les fils fins (fils émaillés), avec l'avantage qu'ils se dénudent d'eux-mêmes au moment du soudage.
4.13.4 Autres élastomères
Le copolymère obtenu par la réaction de molécules d'éthylène et de propylène en concentrations molaires égales est connu sous le sigle EPR (Ethylene-Propylene-Rubber) (fig. 4.63).
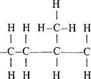
Fig. 4.63 EPR.
La formule ne présente pas de double liaison. Il en résulte une excellente résistance du matériau à l'oxydation, également en présence d'ozone, et le fait qu'il faut recourir à un peroxyde pour provoquer la réticulation. La résistance de l'EPR aux décharges partielles est excellente, ses autres propriétés électriques, satisfaisantes.
En ajoutant à l'EPR, dans une concentration molaire de 2 à 3% un diène (hydrocarbure possédant une double liaison) du type représenté à la figure 4.64, on obtient un EPDM (Ethylène-Propylène Diène Modifié). Ses qualités électriques sont pratiquement identiques à celles de l'EPR lorsqu'il est réticulé au moyen d'un peroxyde. Elles sont inférieures si la réticulation se fait au soufre, procédé rendu possible par la double liaison du diène. L'avantage de l'EPDM sur l'EPR est une réticulation plus rapide et un meilleur état de surface. Ces élastomères sont largement utilisés pour la fabrication d'accessoires injectés, utilisés dans le domaine de la haute tension.
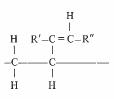
Fig. 4.64
4.14 THERMODURCISSABLES
4.14.1 Polyesters non saturés
Les acides organiques les plus importants sont les acides carboxyliques. Ils sont formés d'un groupement carboxyle (fig. 4.65), lié à un groupement alkyle ou aryle.
Les esters sont des dérivés d'acides carboxyliques dans lesquels l'atome d'hydrogène est remplacé par un groupement alkyle ou aryle, identique ou différent de celui de l'acide. On obtient ainsi diverses familles d'esters (fig. 4.66). Ces esters sont dits non saturés car le groupement carboxyle est non saturé.
![]()
Fig. 4.65
![]()
Ester aliphatique Ester aromatique Ester mixte
Fig. 4.66
La polymérisation d'esters et la copolymérisation d'esters avec d'autres monomères donne une grande variété de produits désignés par le terme général de polyester. Le polyester au styrène (fig. 4.67) est fréquemment utilisé en électrotechnique. Sa résine est formée d'un polyester non saturé, de haut poids moléculaire, en suspension dans du styrène. Ce dernier étant lui-même non saturé, les liens de valence nécessaires à la réticulation sont fournis par les deux constituants de la résine.
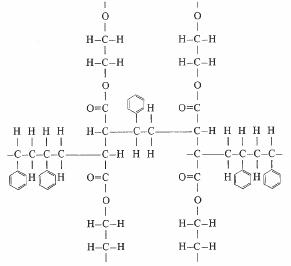
Fig. 4.67 Polyester au styrène. On reconnaît, verticalement deux chaînes de polyester, horizontalement, un groupement styrène et deux amorces de chaînes de polystyrène.
Le durcisseur est-un peroxyde organique, par exemple le peroxyde de benzoyle. La réticulation prend normalement plusieurs heures. Ce temps peut être réduit à quelques minutes par l'emploi d'accélérateurs accroissant la rapidité de décomposition du peroxyde, et donc la libération de ses radicaux libres. Une élévation de température a le même effet, mais moins marqué. Les polyesters sont mis en uvre par moulage, couplage ordinaire, coulage centrifuge pour la fabrication de tubes, trempage, enrobage.
Diverses charges peuvent être ajoutées, telles que la craie, le kaolin, la chaux, la poudre de quartz, les fibres de verre, etc.
La permittivité et les pertes diélectriques dépendent fortement de la nature des charges, et des conditions de réticulation. En basse fréquence, les pertes du polyester chargé de fibres de verre sont supérieures à celles du polyester pur, bien que tan δ soit plus faible dans le verre que dans le polyester. Ce fait doit être attribué à la polarisation interfaciale apparaissant aux surfaces de séparation verre-polyester. La résistance aux courants superficiels est bonne.
Hautement réticulé, le polyester est cassant. Des nuances souples peuvent être obtenues en limitant la réticulation (faible quantité de peroxyde) et par l'adjonction de certaines charges. Il brûle en dégageant de la suie et une odeur douçâtre caractéristique du styrène. Il propage la flamme, mais, chargé de paraffine chlorée par exemple, il peut être rendu autoextinguible. Il est faiblement hygroscopique et sa stabilité chimique est bonne.
Le polyester est utilisé dans la fabrication de grosses pièces isolantes : mats d'antennes légères, protection d'antennes, armoires de commutation, de distribution de câbles, boîtiers divers.
4.14.2 Polyphénols
On peut considérer les phénols comme des dérivés de l'eau, dans laquelle l'un des
atomes H est remplacé par un groupement aryle (fig. 4.68).
![]()
Fig. 4.68 Phénols.
Le plus simple de ces phénols, celui dans lequel Ar est un groupement phényle, porte le nom de phénol. Lorsque Ar est un groupement tolyle, on obtient un crésol. Il y a trois types de crésols (fig. 4.69), correspondant aux trois types de tolyles :
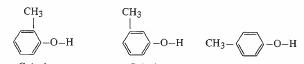
o-Crésol m-Crésol p-Crésol
Fig. 4.69
Les polyphénols sont créés par réaction d'un mélange de phénols avec le formaldehyde. Dans le cas particulier où l'on utilise du phénol pur, on obtient le plus ancien et le plus connu des polyphénols : la bakélite (fig. 4.70).
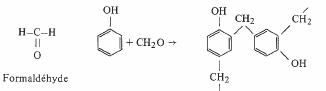
Fig. 4.70 Représentation schématique de la réaction de formation de la bakélite.
Les mélanges de phénols et de crésols sont très largement utilisés, et donnent des macromolécules semblables à celle de la bakélite. Les polyphénols sont utilisés principalement pour l'imprégnation des matières fibreuses: tissus, papiers, bois (anciennement amiante). Cette imprégnation se fait à partir de solutions aqueuses ou alcooliques. De petites pièces sont produites en polyphénols purs.
Les propriétés électriques satisfont aux exigences courantes, mais la résistance aux courants superficiels est médiocre. Un caractère hygroscopique assez marqué rend l'emploi en atmosphère humide problématique. Les tissus imprégnés possèdent de bonnes propriétés mécaniques : haut module d'élasticité, bonne résistance à la traction, à la flexion et au choc. Ils se laissent usiner par les moyens conventionnels. Ils sont chimiquement stables et résistent bien à l'alcool, à l'acétone, à la benzine et aux huiles. Ils supportent moins bien les acides et les bases, ce dont il faut tenir compte dans la fabrication des circuits imprimés. Enfin, les polyphénols sont bon marché et cette caractéristique est à l'origine de leur emploi à si grande échelle.
Ils servent à la confection de corps de bobinage, de circuits imprimés de qualité courante, de pièces d'isolation pour relais électromécaniques, etc. En haute tension, leur résistance à l'huile et aux sollicitations mécaniques en font des matériaux de choix pour les pièces isolantes des disjoncteurs et des transformateurs de puissance.
4.14.3 Polyépoxydes
Les résines polyépoxydes sont ainsi nommées car elles sont formées de molécules linéaires terminées par des groupes époxydes (fig. 4.71).
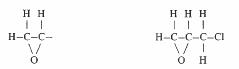
Groupe époxyde Epichlorhydrine
Fig. 4.71 Fig. 4.72
Entre ces groupes, obtenus le plus souvent au moyen d'épichlorhydrine (fig. 4.72), on peut intercaler d'autres groupements provenant de divers dérivés de phénols, par exemple le dihydroxydiphenylpropane (fig. 4.73), dont les atomes hydrogènes des groupes hydroxyles se combinent au chlore de l'épichlorhydrine, formant HC1 neutralisé par le milieu basique où l'on provoque la réaction.
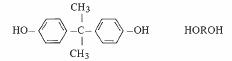
Fig. 4.73 Molécule de dihydroxydiphenylpropane et sa représentation abrégée.
La molécule de résine polyépoxyde se présente alors sous la forme décrite à la figure 4.74.
![]()
Fig. 4.74
Deux types de durcisseurs peuvent être employés. Les premiers sont des amines, ils provoquent la réticulation à température ambiante. Les seconds sont des acides organiques, ils ne produisent la réticulation qu'après un chauffage de la résine à une température comprise entre 140C et 200C selon les cas. Les polyépoxydes durcis à chaud présentent les meilleures propriétés électriques et la meilleure résistance à la chaleur. A température ambiante, le stockage des résines ne devrait pas excéder un an, en raison de l'instabilité des groupes époxydes.
A la variété des produits résultant du nombre de composants différents que l'on peut intercaler entre les groupes époxydes s'ajoute celle qui découle de l'emploi de charges. Ces dernières permettent de modifier les propriétés mécaniques, dans le sens d'un durcissement ou au contraire d'un assouplissement de la matière. Les charges minérales (quartz, mica, alumine), utilisées jusqu'à une concentration représentant 2 à 2,5 fois le poids de la résine permettent de diminuer le coefficient de dilatation de la matière durcie de moitié environ. Ainsi réduit, ce coefficient représente encore 2,2 fois celui de l'acier environ, d'où le risque de fissures dans les assemblages métaux-polyépoxydes.
L'adhérence des polyépoxydes sur les métaux, les céramiques, le mica, est excellente. Sauf modification par les charges, la permittivité et les pertes diélectriques sont pratiquement indépendantes de la fréquence. La résistance aux alcools, huiles, à la benzine, aux acides et bases faibles, à l'eau, est assez bonne. Les polyépoxydes ne résistent pas à l'acétone ni aux hydrocarbures chlorés. Certains d'entre eux ne résistent pas aux intempéries ni aux courants superficiels.
Sous forme de matière première, ils sont mis en oeuvre par coulage ou rempage.Le retrait durant la réticulation, de 2 à 3%, est faible par rapport à d'autres thermodurcissables (polyester : jusqu'à 10%) et peut être abaissé à moins de 0,1 % au moyen de charges et en contrôlant avec précision la température au cours du durcissement. Les polyépoxydes s'obtiennent sous forme de semi-ouvrés, généralement stratifiés : plaques et tubes. Leur domaine d'application englobe les protections d'antennes, y compris les radômes, les éléments de traction des isolateurs en matières plastiques, l'isolation des encoches des grosses machines, certaines pièces de disjoncteurs, les substrats pour circuits imprimés, la protection mécanique de composants électroniques.
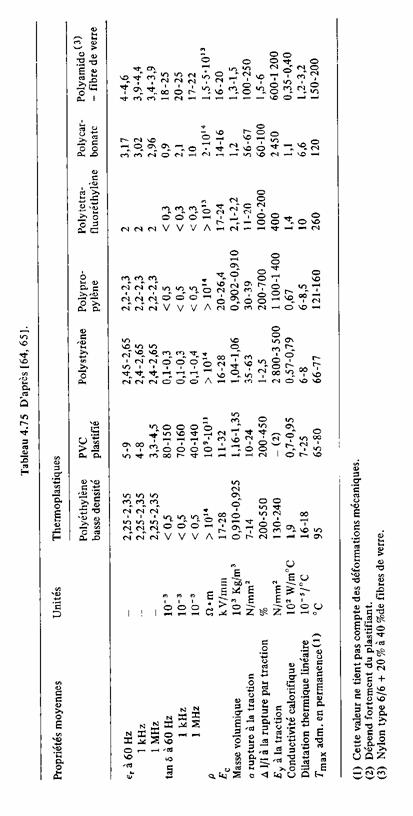
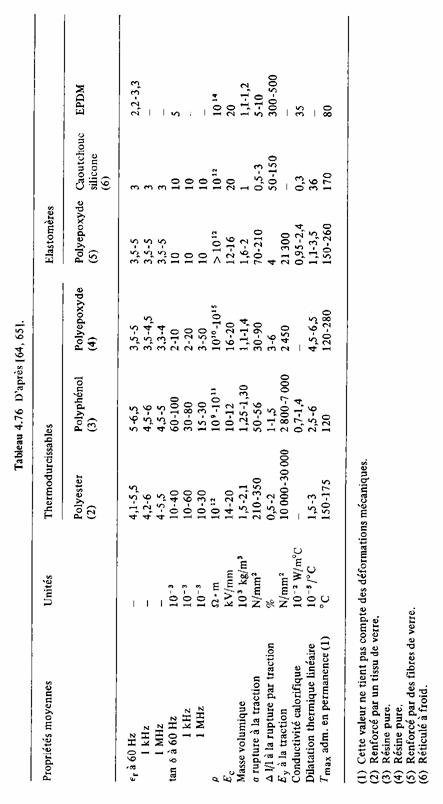
4.15 TABLEAUX DE PROPRIETES DIELECTRIQUES
Les propriétés les plus importantes des polymères usuels sont indiquées aux tableaux 4.75 et 4.76.