
|
|
back
MENU
|
|
Private
|

Energy level
Les énergies de Fermi des différents matériaux sous forme solide sont données dans la table suivante:
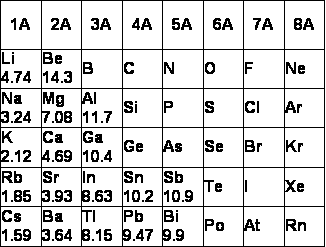
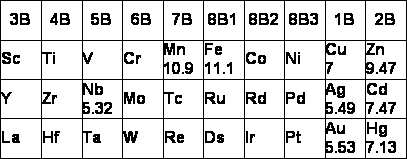
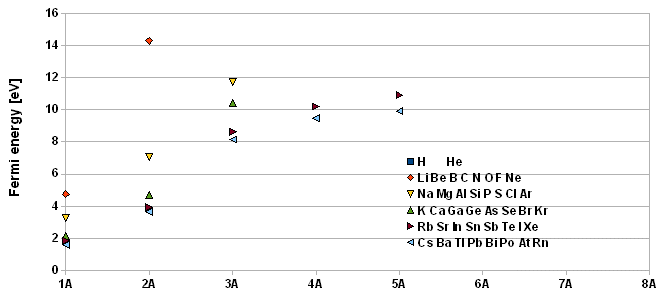
Ces données sont rassemblées dans le graphique suivant qui met en évidence que l'énergie de Fermi augmente en se déplaçant dans le tableau de Mendeléev vers la droite et vers le haut. Ceci peut être facilement expliqué par le fait que la densité électronique suit la même variation, car la dimension des atomes décroît dans les mêmes directions. Finalement comme kF3 est proportionnel à la densité électronique, il apparaît que l'énergie de Fermi varie comme la densité électronique.
Le travail de sortie est l'énergie qu'il faut fournir à un électron pour le l'amener de la surface du métal jusqu'à l'infini. Les valeurs du travail de sortie des électrons de la surface d'un métal sont données dans le graphique qui suit. Le travail de sortie décroît lorsque la taille des atomes augmente. Cela peut être interprété par le fait que les électrons sont plus éloignés du noyau et sont moins fortement liés.
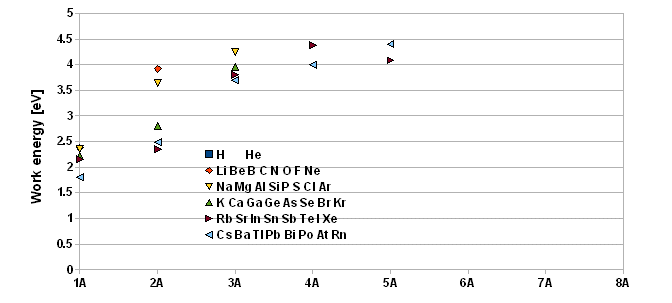
Il est intéressant de mettre ces résultats en rapport avec les énergies de ionisation des électrons dans un gaz d'atomes.
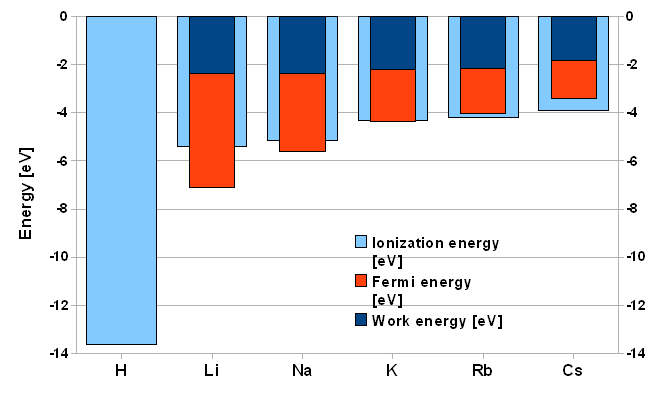
On
remarque que pour les atomes de la première colone (alcalins),
il y a une relative bonne corrélation entre l'énergie
de ionisation d'un atome sous forme gazeuse et l'énergie du
travail de sortie. A nouveau on peut effectuer le rapprochement avec
ce que l'on sait du principe de Pauli. Les électrons n'ont pas
le droit de se trouver dans un même état quantique. Par
conséquent, les électrons de conduction qui sont
délocalisés dans tout le
volume du métal doivent prendre des énergies légèrement
différentes les unes des autres. En première
approximation, elles se répartissent autour du niveau
électronique de l'atome isolé. Il est bien entendu que
en pratique les valeurs numériques dépendent de la
structure cristalline, de l'orientation de la surface, etc.
Si l'on examine le cas du lithium, on voit qu'il faut fournir 5.4 [eV] à l'électron périphérique pour le faire quitter l'atome isolé et 2.2 [eV] à l'électron dans le niveau de Fermi pour le faire quitter la surface du solide.
Les chimistes ont pour habitude de donner les énergies de ionisations des atomes en [kJ/mol]. En d'autres termes, ils donnent l'énergie qu'il faut fournir à une mole d'électrons d'atomes gazeux pour les amener à l'infini.
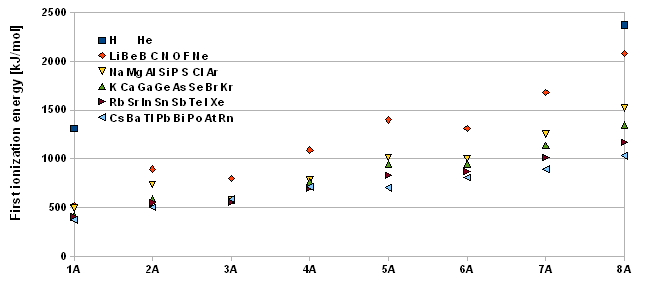
Pour
le lithium l'énergie de première ionisation est de 521
kJ/mol.
Sachant qu'il y a A = 6.02 x 1023 atomes dans une mole, que la charge de 1 électron est de e = 1.6 x 10-19 Coulomb, que l'électron-volt est l'énergie électrique WE de l'électron soumis à une tension de 1 Volt (WE = e U), il est possible de transformer les énergies données de [kJ/mol] en [eV].
Energie 1 électron [eV] = 1000 Energie d'une mole d'électrons [kJ/mol] / (A e).
En faite Ae = 96500 [C/mol] n'est rien d'autre que la constante de Faraday, la charge d'une mole d'électrons.
Pour le Li, les 521 kJ/mol correspondent à une énergie de 5.4 [eV].
Dans un gaz Li+ + e- (l'atome ionisé + électron) possèdent une énergie de 5.4 eV plus élevée que celle de l'atome de Li.
Source: Garmanage: Roland Gallay